

Účelem vzdělání není zaplnit mysl, ale otevřít ji. Čím více poznatků si osvojíme, tím víc si uvědomíme, co ještě neznáme.

Literatura
Apoferritin molekula pro nanomodicínské technologie šetrnější léčby nádorů
 1. Ferritin a příprava apoferritinu
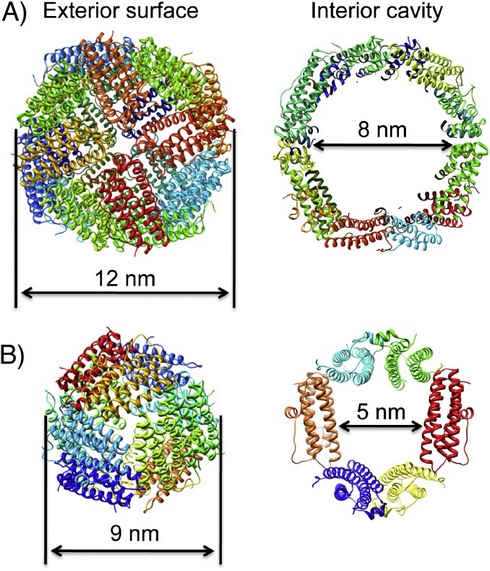
1. Ferritin a příprava apoferritinu
Ferritin je protein a byl objeven v roce 1937 Laufbergerem, který jej izoloval z koňské sleziny a zjistil, že obsahuje až 23 % železa. Molekuly ferritinu jsou obsaženy ve většině živých organizmů a slouží k uskladnění iontů železa v podobě hydratovaných hydroxid-oxidů železitých. Zabrání se tak toxicitě, která by byla způsobena tvorbou volných radikálů při redukci železitých iontů na ionty železnaté. Jsou známy dva druhy ferritinů, a to maxiferritiny a miniferritiny. Tyto ferritiny mají rozdílné vnější a vnitřní rozměry a molekulové hmotnosti. Maxiferritiny se skládají z 24 polypeptidových jednotek, mají vnější rozměr 12 nm, dutina je o průměru 8 nm a molekulová hmotnost je 480 kDa. Miniferritiny jsou pak složeny ze 12 polypeptidových jednotek s vnějším rozměrem 8 nm, průměrem dutiny 5 nm s hmotností 240 kDa. K výzkumným účelům se většinou používají maxiferritiny. Ty jsou komerčně dostupné a jejich schopnost reverzibilně skladovat a uvolňovat ionty železa upoutala značnou pozornost vědců. Apoferritin se připraví z ferritinu redukčním rozpouštěcím procesem za použití thioglykolové kyseliny nebo dithioničitanu. Dialýza za přídavku některého z redukčních činidel se opakuje, dokud se nezíská žlutý roztok apoferritinu. Tato výměna iontů je umožněna přítomností 14 kanálků ve struktuře apoferritinu, z nichž je šest hydrofobních a osm hydrofilních.
 2. Jak lze využít apoferritin?
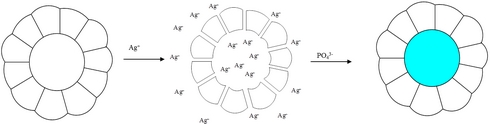
2. Jak lze využít apoferritin?
Apoferitin v elektrochemii
Důležité je, že apoferritin je schopen ve své dutině uskladnit i další ionty a změnou vlastností prostředí je uvolnit. Pro syntézu nanočástic uzavřených v apoferritinu se využívá kanálků ve struktuře apoferritinu pro vyplnění dutiny potřebnými ionty a následného přídavku reagentů k vyvolání chemické reakce. V tomto případě je apoferritin využit jako nanoreaktor.
 Apoferitin pro biologickou aplikaci
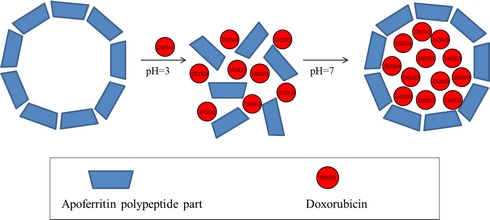
Apoferitin pro biologickou aplikaci
Druhou možností syntézy je využití rozevření struktury při nízkém pH, kdy se k polypeptidovým jednotkám v roztoku následně přidá látka, kterou chceme do apoferritinu uzavřít. Přídavkem roztoku hydroxidu se docílí zvýšení hodnoty pH, kdy se dostane požadovaná látka dovnitř apoferritinové struktury. Poté následuje dialýza, kdy se odstraní přebytek látky vně apoferritinu.
3. Využití v zobrazování a medicíně, další možnosti
Dutina v apoferritinu může být využita pro úschovu iontů nebo molekul a je použitelná pro přípravu nanočástic s definovatelnou velikostí.
 Zobrazování
Zobrazování
Apoferritin skýtá velké možnosti pro přípravu široké řady materiálů, které mohou být použity nejen v medicíně, ale rovněž pro elektronické aplikace. Pro účely zobrazování byly v apoferritinu připraveny kvantové tečky např. CdS, CdSe, ZnSe a tečky PbS s detekcí emisního spektra v blízké infračervené oblasti. Komplexy lanthanoidů uzavřené v apoferritinu byly pro změnu studovány jako kontrastní látky pro zobrazování magnetickou rezonancí.
Šetrnější léčba
Apoferritin lze rovněž použít k uzavření protinádorových léčiv, jako jsou cisplatina, karboplatina, oxaliplatina nebo epirubicin a doxorubicin.
Další velkou výhodou apoferritinu, kterou lze využít pro transport léčiv, je možnost modifikace jeho povrchu. Povrch apoferritinu může být modifikován biotinylem, protilátkou nebo dalšími organickými a anorganickými činidly. Dále je možné využít spojení biotinu a streptavidinem modifikované superparamagnetické částice a transportovat apoferritinové komplexy do požadované tkáně pro zobrazovací nebo léčebné účely vnějším magnetickým polem. Modifikace umožňují využití pro transport uzavřených léčiv k cílovým buňkám mnohem efektivněji s minimalizací vedlejších účinků, zvláště pak toxicity vůči necíleným orgánům.
Vydání sborníku:Světový den boje proti rakovině 2013-World Cancer Day
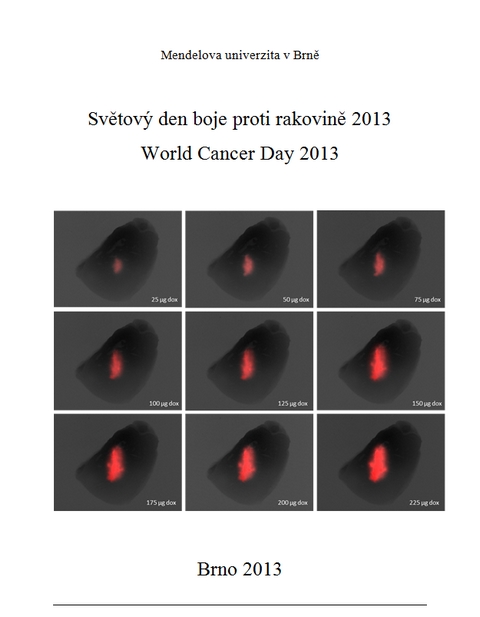 U příležitosti Světového dne rakoviny byl vydán sborník v nákladu 60 ks, ISBN: 978-80-7375-702-1. Ve sborník obsahuje abstrakty prezentovaných prací.
U příležitosti Světového dne rakoviny byl vydán sborník v nákladu 60 ks, ISBN: 978-80-7375-702-1. Ve sborník obsahuje abstrakty prezentovaných prací.
Kizek (WCD_01): Nádorová onemocnění jako závažný celospolečenský problém
Adam (WCD_02): Metalothionein jako potencionální nádorový marker
Nedecký (WCD_03): Metalothionein a jeho role v metabolismu kyslíkových radikálů
Vaculovičová (WCD_04): Na nanotechnologiích založené zobrazovací techniky v diagnostice nádorů
Nejdl (WCD_05): Změny struktury DNA po vazbě platinových cytostatik
Gumulec (WCD_06): Meta-analýza vztahu zinečnatých iontů k nádorovým onemocněním
Tmejová (WCD_07): Hladiny metalothioneinu u dětí se zhoubnými nádory
Zítka (WCD_08): Sledování interakcí protinádorového léčiva doxorubicinu s aminokyselinami
Masařík (WCD_09): Nové nádorové markery u nádorů prostaty
Hynek (WCD_10): Elektrochemické metody v nádorové diagnostice
Tmejová (WCD_11): Metalothionein – nový nádorový marker
Konečná (WCD_12): Atomová absorpční spektrometrie jako nástroj pro sledování iontů kovů
Cernei (WCD_13): Sarkosin, nádorový maker z moči
Nejdl (WCD_14): Nanočástice oxidu železitého jako nový marker onkologických onemocnění
Nedecký (WCD_15): Imunologická analýza nádorových markerů
Chudobová (WCD_16): rychlá diagnostika bakteriálních a virových infekcí u nádorových onemocnění
Blažková (WCD_17): Detekce doxorubicinu ve svalové tkáni
Kopel (WCD_18): Apoferitin jako moderní nástroj pro cílenou terapii
Nguyen (WCD_19): Behavior of cisplatin investigated by spectrophotometry and capillary electrophoresis
Šmerková (WCD_20): Izolace, charakterizace a polymerázová řetězová reakce u nádorových onemocnění
Šmerková (WCD_21): Určení primární sekvence, základní informace pro nádorovou diagnostiku
Merlos Rodrigo (WCD_22): Two-dimensional electrophoresis and mass spectrometry for cancer protein identification
Sborník je k dispozici na internetových stránkách a v tištěné podobě u vydavatele.
ODKAZY | LINKS




NOVÉ PUBLIKACE
Quantum Dots:Biological and biomedecical applications
Archiv
23_201322_2013
21_2013
20_2013
19_2013
18_2013
17_2013
16_2013
15_2013
14_2013
13_2013
12_2013
11_2013
10_2013
09_2013
08_2013

 | Zemědělská 1/1665 613 00 Brno Budova D | Tel.: +420 545 133 350 Fax.: +420 545 212 044 |  |
 |

















