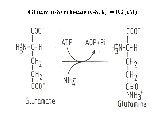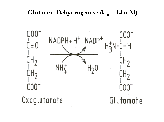dusík
| asimilace dusíku | inkorporace dusíku | translokace dusíku | symptomy nedostatku a nadbytku dusíku | |
||
|
Asimilační cesty dusíku vycházejí z N2, nitrátů,
amoniaku nebo organických N sloučenin. Všechny poskytují buňce
buď po přeměně (nitráty) nebo přímo amoniak, který je v převážné
míře v buňce utilizován po reakci s oxokyselinami na
aminokyseliny.
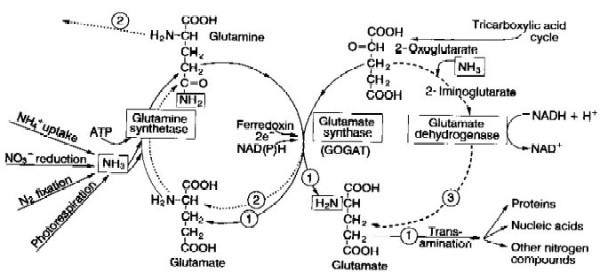
U vyšších rostlin byla prokázána cesta zabudování
amoniaku enzymovým systémem GS/GOGAT (glutaminsyntetázou/glutamin
2-oxoglutarátaminotransferázou, tj. glutamátsyntázou). Uvedená
reakce probíhá v chloroplastech spřaženě za sebou a výsledným
produktem je glutamin a glutamát (obr. 3.7).
Glutaminsyntetáza (GS) vyvolává reakci, při níž glutamát
funguje jako akceptor NH3 za vzniku glutaminu. Reakce je
endotermní a vyžaduje ATP a Mg2+. ATP je dodáván
fotosytetickou fosforylací. V přítomnosti redukčního zdroje předává
glutamin svoji aminoskupinu a-oxoglutarátu.
Reakci katalyzuje enzym glutamátsyntáza a energii dodává
ferredoxin. Schéma inkorporace amoniaku (1,2) Glutaminsyntetáza (GS) při nízké hladině amoniaku (1), resp. při vyšší hladině amoniaku (2). Působení glutamátdehydrogenázy (3) (Marschner, 1995)
Přítomnost glutaminsyntetázy v chloroplastech zaručuje,
že amoniak vzniklý po redukci nitrátu může být utilizován,
aniž by došlo k přerušení fosforylace. Lee a Miflin (1974) předpokládají,
že tento systém představuje nejdůležitější cestu asimilace
NH3 v zelených rostlinách, a přitom nevylučuje roli
glutamátdehydrogenázy (GDH). Řada pokusů nás poučuje o tom, že
i když za normálních podmínek probíhá asimilace amoniaku
cestou GS (GOGAT) mají rostliny poměrně vysoký potenciál glutamátdehydrogenázy.
To vede k domněnce o existenci jakéhosi bezpečnostního zařízení
rostliny, když nejsou splněny vyšší energetické nároky.
Glutamátdehydrogenáza katalyzuje reakci mezi NH3
a a-oxoglutarátem.
Proces má za následek aminaci a-glutarátu
spojenou s redukcí NADHP (redukční aminace). Součástí tohoto
enzymu je Zn.
V glutamátu a glutaminu vázaný aminový dusík může být
přenášen na jiné oxokyseliny transaminací. Tento proces
katalyzují aminotransferázy. Transaminace je u rostlin prostředkem
pro syntézu celé řady aminokyselin a je pravděpodobné, že NH2
skupiny většiny aminokyselin jsou právě odvozeny od glutamátu.
Má-li rostlina nadbytek NH3, mohou glutamát a
asparát sloužit jako akceptory amonia. Vytvoření amidů je pro
rostliny důležité, poněvadž nahromaděný NH3 v
pletivech by působil na rostliny toxicky. Toxicita je způsobena tím,
že amoniak silně alkalizuje prostředí, což se projevuje
vystouplou listovou nervaturou a zasycháním listů od špiček. Na
to pak navazuje blokování fotosyntetické fosforylace, omezení dýchání,
inhibice enzymových systémů. Kritická koncentrace toxicity NH3
je uváděna v rozpětí kolem 0,15-0,2 mM pro kořeny. Hromadění
asparaginu a glutaminu nastává tehdy, jsou-li rostliny vystaveny
vysokým dávkám anorganického dusíku, zejména NH4+.
Amoniakální dusík je dobře asimilován těmi rostlinami,
které mají dostatek sacharidů, důležitých pro tvorbu organických
kyselin. Při naprostém jejich nedostatku se nehromadí jen amidy,
ale i amoniak a dochází k otravě rostlin. Proto je opodstatněný
názor, že na počátku růstu rostlin jsou amnné soli méně
vhodným zdrojem dusíku než v pozdější době, kdy fotosyntézou
vzniká dostatečné množství sacharidů. |
||
|
autor textu: Prof. Ing. Rostislav Richter, DrSc. |
||
Poslední aktualizace: 23.01.2004 08:41
Ústav agrochemie a výživy rostlin, MZLU v Brně, Zemědělská 1, 613 00 Brno