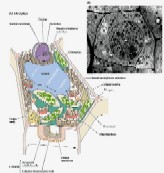
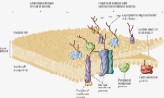
Příjem živin kořeny
| mechanismus příjmu a transportu látek v rostlině | transport na krátké vzdálenosti | transport na střední vzdálenosti | dálkový transport | |
||
|
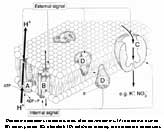
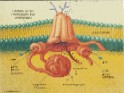
Látky, které mají přejít z vnějšího prostředí do buněčného, musí nutně překonat rozhraní buňky reprezentované zpravidla plazmalemmou. Přes plazmalemmu se látky dostávají aktivně nebo pasivně. Existují i vyjímky, zvláštní pozornost si zasluhují procesy pinocytózy. Tento transport je sice neselektivní, ale může být velmi výkonným. Dále sem patří i přechod látek ze sousedních buněk systémem plazmodezmů - přímých spojek mezi protoplasty (symplastická cesta). Vraťme se k transmembránovému transportu jako k základní formě komunikace buněk obecně s vnějším prostředím. Mezi látky, které sledujeme, patří především minerální složky rostlinného těla nebo ty, které v minerální formě do buňky vstupují (zpravidla v iontové formě). Řada látek do buňky difunduje - tedy vstupuje pasivně. I v tomto případě může být v cestě difúzi nějaký filtrační systém (iontově selektivní kanály), který vede k určité „selektivitě“ - ovšem dokud se neanuluje hnací síla pro všechny složky tohoto systému, pak musí být výsledkem vždy rovnováha. Pasivně vstupují i látky, které procházejí lipidní vrstvou membrány. Transport na krátké vzdálenosti v sobě zahrnuje základní mechanismus sycení symplastu, tj. vnitřního cytoplamatického systému z vnějšího prostoru, a proto celkový tok je závislý na povrchu protoplastu. Další významnou složkou buňky je vakuola, kolem níž se vyvíjí tonoplast. Ten je sídlem aniontových transportních systémů a systémů pro transport organických látek. Tonoplast je dobře permeabilní pro kationty (zvláště K+), proto se vyrovnává nadbytek organických kyselin ve vakuole právě pasivní distribucí K+ iontu z cytoplazmatického prostoru. Tedy ve vakuole se hromadí ve zvýšeném množství jak anionty, tak kationty, které je potom doprovázejí, a tím celková koncentrace bude vyšší než v cytoplazmě a než ve vnějším prostředí. To vyvolává jevy, které vedou k osmotickým efektům v rostlinné buňce. Výsledkem toho je stav, že jak za kationty, tak za anionty se vyměňují iontové produkty vody (H+, OH- + CO2 ---> HCO3-), které vyloučeny z buňky se opět vrací do nedisociované formy - vody. Z buňky ven se vylučuje sumárně voda a dovnitř vstupují soli. Soli mají osmotickou aktivitu, zatímco molekuly rozpouštědla ne. Vzniká tedy neustále přetlak osmoticky aktivních látek uvnitř rostlinné buňky, a tím dochází k intenzivnímu nasávání vody, zvětšuje se její objem a stoupá turgor. To vyžaduje existenci pevné stěny buněčné s určitou elasticitou. Membrány cytoplazmy rostlinné buňky nejsou během celého vývoje konstantní - mění se. V období objemového růstu se povrch buňky zvětšuje, zvětšuje se plazmalemma, vakuola a tonoplast. Právě díky hromadění K+ iontu v cytoplazmě a ve vakuole dochází k permanentnímu zvyšování turgoru v buňce, který je pracovním mechanismem při zvětšování jejich objemu. Přirozený buněčný turgor je současně základem prostorového rozmístění všech bylinných orgánů rostliny a mluvíme o turgescenci jakožto stavu rostliny s dostatkem vody, solí atp. Zde je i přímá vazba k jiným funkcím rostliny, jako je fotosyntéza a příjem živin kořeny. Uvedené mechanismy nejsou podrobně prostudovány. Víme jenom, že nemůžeme dosud jednoznačně konstatovat, kdy a za jakých podmínek je rostlina schopna vytvořit vysoké koncentrační gradienty mezi vnějším a vnitřním prostředím, a kdy to přímo souvisí s potřebami metabolismu, a kdy je to vedlejší produkt těchto dějů. Vysoce efektivní a selektivní formy transportu jsou zřejmě obecně vázány na funkci metabolických procesů (na spotřebu energie z disimilačních procesů, případně z fotosyntézy). Jedná-li se o orientovaný transport z vnějšku dovnitř, dochází ke značným koncentračním diferencím mezi vnějším a vnitřním prostředím, který se projeví akumulací přijatých látek. Dosažení určité koncentrace látek (iontů) ve vnitřním vakuolárním roztoku není výsledkem postupného hromadění, ale dynamickou rovnováhou mezi tokem do buňky a výtokem do vnějšího prostředí. Její úroveň se stabilizuje pro každý iont na jiné hodnotě. Kvalita těchto transportních systémů se podle Dvořáka (1989) mění podle polohy buněk (pletiv) v témže orgánu. Některé ionty, např. vápenaté, mohou membránu stabilizovat, zvyšovat její semipermeabilitu, zatímco v jiných případech (ionty těžkých kovů) mohou membránu narušovat a zvyšovat její permeabilitu (např. K+ v koncentraci nad 10-3 M). Existence membrány je tedy podmínkou, aby mohly vynikat rozdílné koncentrace iontů mezi vnějším a vnitřním prostředím, ale současně musí být tento efekt energeticky zajištěn. Na něm se podílí energetický metabolismus ať z respiračních zdrojů nebo přímo z fotosyntézy. Přitom energie může být využita buď na aktivní transport (na práci přenašeče) nebo na syntézu transportérů (chelatizačních látek). Vůči všem transportovaným kationtům je obecně kompetitivní proton (H+) oproti aniontům opět OH- nebo HCO3-. Pokud jde o aktivní transport iontů, potom zpravidla převládá transport kationtů (především K+). Rozdíl elektrostatických aniontů je doplňován z organických kyselin (tvorbou kyseliny jablečné, kyseliny citronové). K tomu slouží fosfoenolpyruvátkinázá, případně další enzymy vázané v tonoplastu. Tyto procesy vedou k biologickému pufrování cytoplazmy. Jejím úkolem je udržovat pH na neutrální hodnotě nezávisle na pH okolních kompartmentů. regulace pH v buňce funguje na principu „biochemického pH - statu“. Zvýšení pH v cytoplazmě (> produkcí OH- při redukci NO3-) je způsobené syntézou silných kyselin (malát) z fosfoenolpyruvátu (PEP) za účasti PEP-karboxylázy. Snížením pH cytoplazmy (produkcí H+) se aktivuje malátový enzym, který dekarboxyluje malát a do prostředí kořene se uvolňuje CO2 a OH-. Dekarboxylací malátu vznikne pyruvát a z něho neutrální produkt. Optimum cytoplazmatického pH (elektroneutralita) se tedy udržuje v mezích činností dvou enzymů (PEP-karboxyláza a malátový enzym). Příjem a transport iontů v kořeni je selektivní proces. Kořeny rostlin se musí přizpůsobit různým exogenním koncentracím iontů tak, aby byla zabezpečena vhodná endogenní koncentrace i vzájemný poměr iontů v buňkách. V kořeni rostlin tedy probíhá intenzívní metabolismus, který je nutný k resorpci iontů. Vzhledem k tomu, že ve vakuolách kořenových buněk je koncentrace iontů vyšší než koncentrace iontů v tekuté půdní fázi, musí probíhat příjem živin proti koncentračnímu spádu, což je spojeno se spotřebou energie. Kořenové buňky musí mít k dispozici selektivní mechanismus příjmu živin, neboť jsou odkázány u celé řady živin na jejich velmi nízké koncentrace v půdním roztoku a na druhé straně je jim nabízena i relativně vysoká koncentrace prvků, které rostlina nezbytně potřebuje. Pro každou živinu je zapotřebí, aby byla v půdním roztoku dosažena alespoň její mezní koncentrace, jinak by její příjem mohl být omezen tak, že by se na rostlině začaly objevovat příznaky jejího nedostatku. Mezní koncentrace jsou pro jednotlivé živiny rozdílné. Transport iontů do buňky přes semipermeabilní membrány musí být aktivní a děje se pomocí přenašečů bílkovinné povahy. Důvodem této hypotézy je skutečnost, že koncentrace některých iontů v buňce převyšuje jejich obsah ve vnějším prostředí 1000-10000x. Z toho bylo odvozeno, že musí existovat mechanismus, který umožňuje transport iontů přes membránu ve směru gradientu jejich koncentrace. Studiu mechanismu transportu iontů se věnovali Epstein a Hagen (1952), kteří předpokládali existenci dvou rozdílných transportních systémů závislých na koncentraci iontů v prostředí. V buněčných membránách jsou dva typy bílkovinných přenašečů, které jsou pro každý iont specifické v závislosti na nízkých koncentracích (< 1 mmol.l-1), tzv. systém I, a na vysokých koncentracích(> 1mmol.l-1), tzv. systém II. Podle nejnovějších poznatků v plazmalemmě při nízkých koncentracích iontů jsou v činnosti jen mechanismy systému I s vysokou afinitou k iontům. V systému II při vysokých koncentracích iontů v půdním roztoku je systém I odpojený, ionty se transportují difúzí přes plazmalemmu a nosič funguje v tonoplastu. Předpokládá se, že mechanismy jednoho systému působí při jedné a druhého systému při druhé membráně (viz obrázek). Lokalizace mechanismu příjmu iontů (podle Nissena 1973)
Snahou každé živé buňky je zachovat si poměr (stechiometrický) mezi syntézou organických kyselin a uvolňováním H+ z buňky na udržení její elektroneutrality. Proto je pochopitelné, že regulace pH v buňce se přímo spojuje s metabolismem, při kterém se buď produkuje nebo spotřebovává H+. Metabolické produkty, které obsahují C, H, O a N mají vždy negativní náboj v důsledku převahy karboxylových skupin nad NH3. Přebytek karboxylových skupin musí být vyrovnán anorganickými kationty, aby byl zachován princip elektroneutrality potřebný k tomu, že většina enzymů cytoplazmy vykazuje optimum aktivity pH mezi 6-7. Ve vakuole je pH nižší a pohybuje se v rozmezí 5-6. Citlivost cytoplazmatických enzymů je tak velká, že kontrola pH uvnitř buňky je základní podmínkou metabolismu. Vytěsnění H+ nebo OH- z buňky závisí od toho, jaký iont do ní vstupuje. Při vstupu NO3- nebo SO42- se z buňky uvolňuje OH- a při vstupu NH4+ se vylučuje H+. Vtok NO3- se vybalancuje výtokem OH-. Během respirace buňky pH cytoplazmy klesá v důsledku uvolňování H+, který se transportuje z mitochondrií do cytoplazmy, případně do vnějšího prostředí. Současně se antiportem transportuje dovnitř K+, který zvyšuje turgor a cytoplazmatické pH začne narůstat. Zvýšené pH podmiňuje syntézu organických kyselin (malát), a tím i produkci H+ (COO-, H+). Výměnou za H+/K+ přijatý draslík může neutralizovat kyseliny (K-malát) nebo se ukládá do vakuoly. Syntéza organických kyselin probíhá potud, dokud se vyměňuje vytěsněný proton za K+ anebo než se produkty této syntézy převedou do vakuoly. Toto je pouze příklad možného propojení metabolismu buňky k pH. Změny pH v buňce vedou k produkci H+ nebo OH-, které se uvolňují jako odezva na signály mající původ v metabolismu. Vlastnosti protonu (H+) je schopnost recirkulace, tj. opětovně vstupovat do buňky podle jejího požadavku na neutralizaci volných OH- skupin. Na rozdíl od H+ iontu OH- ionty, které se uvolňují z buňky při zvýšení cytoplazmatického OH, nepodléhají recirkulaci a jsou tedy pro buňku ztracené. Ionty, které vstupují do buňky jsou postupně metabolicky utilizovány, různě zabudovávány a přitom se může měnit jejich iontový charakter (např. z aniontu NO3- se tvoří kationická aminová skupina atp.) a stávají se členy systému cytoplazmy. Řada z nich může být podle potřeby znovu i opakovaně (několikrát) přeměňována a přitom mění svou funkci v organických látkách, ale i v živých systémech. Tyto procesy přeměny látek označujeme jako reutilizaci a jsou běžné při klíčení semen, rašení pupenů, vegetativním množení, ale i v průběhu ontogenetického vývoje rostlin. |
||
|
autor textu: Prof. Ing. Rostislav Richter, DrSc. |
||
Poslední
aktualizace: 24.01.2004 16:30
|
|
Ústav agrochemie a výživy rostlin, MZLU v Brně, Zemědělská 1, 613 00 Brno